覃鲁珊1,2‡,赵海平1,2‡,赵艳玲1,马致洁1,3,曾灵娜1,张雅铭1,张萍1,鄢丹1,柏兆方1,赵奎君3,王伽伯1*,肖小河1*
1 解放军302医院·全军中医药研究所;2 江西中医药大学;3 首都医科大学附属北京友谊医院;
【摘要】 目的:比较大黄总蒽醌与总鞣质提取物对肝脏的保护和损伤双向作用。方法:同时采用正常和病理动物(急性CCl4肝损伤模型),对比考察低、高剂量(5.40、14.69 g生药/kg)的大黄总蒽醌与总鞣质提取物连续灌胃6天对大鼠一般状态、生化指标和肝组织病理的影响。结果:大黄总蒽醌对正常动物各生化指标影响无明显影响,且可以显著降低肝损伤模型大鼠的血清丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转氨酶(AST)、透明质酸(HA)、转化生长因子-β1(TGF-β1),改善肝组织坏死,表明大黄蒽醌对肝损伤大鼠有保护作用。大黄总鞣质高剂量组引起正常大鼠血清AST、ALT、HA显著升高,病理切片可见肝细胞脂肪变性及小片状胆汁淤积,表明大黄鞣质对正常大鼠肝脏有损伤作用;大黄总鞣质对模型大鼠AST、ALT有改善作用,但对HA、TGF-β1无改善作用,且观察到肝组织纤维组织增生加重,表明大黄鞣质加重了模型大鼠肝纤维化。结论:在相当于药材生药量可比的剂量下,大黄蒽醌类成分对肝脏的保护作用显著强于鞣质类成分,而高剂量大黄鞣质具有一定的肝损伤作用,提示大黄在临床治疗肝病时应注意煎煮或提取方式,避免鞣质类成分对疗效的影响和潜在的肝毒性。
【关键词】 大黄;蒽醌;鞣质;肝损伤;保护;纤维化;因子分析
Bidirectional effects of the rhubarb anthraqenones and tannins to rat liver
QIN Lu-shan1,2, ZHAO Hai-ping1,2, ZHAO Yan-ling1, MA Zhi-jie1,3, ZENG Ling-na1, ZHANG Ya-ming1, ZHANG Ping1, YAN Dan1, BAI Zhao-fang1, ZHAO Kui-jun3, WANG Jia-bo1, XIAO Xiao-he1
1 China Military Institute of Chinese Medicine, 302 Military Hospital, Beijing (100039),China; 2 Jiangxi University of Traditional Chinese Medicine, Nanchang (330004),China; 3 Beijing Friendship Hospital, Capital Medical University, Beijing (100050),China
【Abstract】Objective : To comparatively investigate the bidirectional effects of the rhubarb anthraqenones and tannins to rat liver. Method: The total anthraquinone extract (TA) and total tannin extract (TT) of rhubarb were administrated to either normal or carbon tetrachloride(CCl4)-injured rats for 6 days at tow dosage levels ( 5.40 and 14.69 g·kg−1, counted as the quantity of crude material of rhubarb), followed by biochemical and histopathological tests of the rats' livers. Result: After administration of TA, no obvious injury was found in normal rats while protective effect to CCl4-treated rats was observed, with significant decline of values of serum alanine aminotransferase(ALT), aspartate aminotransferase(AST), hyaluronic acid (HA), transforming growth factor β1(TGF-β1) and improvement of hepatic necrosis in histopathology. By contrast, the administration of TT showed paradoxical effects to normal and CCl4-injured rats. In normal rats, TT induced significant increases of values of serum AST,ALT and HA as well histopathological changes including fatty denaturation of liver cells and cholestasis at the high dosage(14.69 g·kg−1). In CCl4-injured rats, TT revealed improvement to serum ALT and AST but not serum HA and TGF-β1, and aggravated the liver fibrosis. Conclusion: At equivalent dosage, the rhubarb anthraquinones had much greater liver protective effect than tannins. The total tannins of rhubarb had toxic effect to liver at high dosage. The results suggested that rhubarb should be used properly in decoction and extraction to reduce tannins and avoid its potential hepatotoxicity and impact to curative effect in clinics.
Keywords: rhubarb;anthraquinone;tannin;liver injury;protection;fibrosis;factor analysis
大黄是临床常用的肝病治疗中药,具有清热泻火、利湿退黄、凉血解毒之功效[1],是肝病常用方药茵陈蒿汤、大黄蟅虫丸等的主要药味。然而,近年来研究发现长期、大剂量使用大黄可致肝、肾损害 [2-4],引起国内外高度关注。笔者前期研究发现,大黄在一定的剂量范围内对肝脏具有双向作用,既可表现出对肝损伤动物的治疗作用,又可表现出对正常动物的肝损伤作用。大黄中具有多种活性成分,主要包括蒽醌类和鞣质类[5-6]。蒽醌在大黄药材中含量在1.5%~4%左右,是药典控制的指标成分;鞣质类成分在大黄中含量较高,可达5~15%。一般认为蒽醌类成分具有保肝作用,但也有报道认为蒽醌具有肝毒性。鞣质的肝毒性尚不肯定,一般认为可水解鞣质的毒性高于缩合鞣质 [7-8]。大黄鞣质主要为可水解鞣质,其是否具有肝毒性尚未见报道。大黄肝保护和肝损伤作用的物质基础有待科学阐明。
为此,本文将大黄蒽醌和鞣质分离开来,对比研究两类成分分别对正常大鼠和肝损伤模型大鼠的作用规律,以期阐明大黄对肝脏保护和损伤作用的物质归属。根据大黄蒽醌类成分极性较弱、易溶于乙醇等有机溶剂,鞣质极性较强、易溶于水的性质特点,在阐明肝保护和肝损伤物质归属的基础上,可以通过选择恰当的提取溶剂和方式提高临床疗效和避免肝脏不良反应发生,促进提高大黄临床科学用药水平。
1.材料与仪器
大黄药材采自甘肃礼县,经解放军第三〇二医院肖小河研究员鉴定为蓼科植物掌叶大黄Rheum palmatum L.的干燥根及根茎。大黄总蒽醌和总鞣质提取物由前期工作制备[9],按文献方法检测总蒽醌[10]和总鞣质[11]含量,总蒽醌提取物中蒽醌含量56.73%、鞣质含量1.78%,总鞣质提取物中蒽醌含量0.83%、鞣质含量38.26%,表明蒽醌和鞣质得到较好分离。前期分析表明,大黄总鞣质提取物主要含没食子酸葡萄糖苷、儿茶素二聚体、没食子酰儿茶素等可水解鞣质衍生物[12];大黄总蒽醌提取物主要含大黄酸、大黄素、大黄酚、芦荟大黄素、大黄素甲醚及其葡糖糖苷等,以及少量番泻苷类成分[13]。
SD大鼠(SPF级,6~8周龄,180±30g,♀♂各半)由中国人民解放军军事医学科学院实验动物中心提供[SCXK-(军)2007-004]。CCl4(20060525,北京北化精细化学品有限责任公司);橄榄油(F20080219,国药集团化学试剂有限公司);TGF-β1试剂盒(090120,北京普尔伟业科技有限公司);其它试剂均为分析纯。
Sn-69513型免疫计数器(上海核所日环光电仪器有限公司);2500 型超声波清洗器 (江苏省昆山市超声仪器有限公司), 旋转蒸发仪(德国Heidolph 公司), 全自动生化分析仪 (OLYMPUS Au 800, 日本), 包埋机(AO,美国), 切片机(AO, 美国),光学显微镜 (Galen TMⅢ, 江南光学仪器厂),DT1000电子天平(中国轻工业机械总公司常熟衡器公司)。
2.实验方法
2.1 实验分组、造模及给药
①分组 将动物预养1周后,随机分为10组,每组10只,♀♂各半:空白组(N)、模型组(M);空白组+大黄蒽醌低剂量组(NA1)、空白组+大黄蒽醌高剂量(NA2)、空白组+大黄鞣质低剂量组(NT1)、空白组+大黄鞣质高剂量组(NT2);模型组+大黄蒽醌低剂量组(MA1)、模型组+大黄蒽醌高剂组(MA2)、模型组+大黄鞣质低剂量组(MT1)、模型组+大黄鞣质高剂量组(MT2)。②造模 模型组在实验的第1天一次性腹腔注射含10% CCl4的橄榄油(2 ml•kg-1体重,现配现用)。③给药 为了保证可比性,大黄总蒽醌和总鞣质均以相当于药材生药量给药。前期研究大黄4个剂量(2、5.4、14.7、40 g生药/kg体重)对正常和肝损伤大鼠的量-效/毒关系,发现5.4和14.7 g生药/kg是大黄双向作用剂量范围[13],故本文以这两个剂量进行实验。各给药组在造模第二天开始灌胃给药,5 ml•kg-1体重,1 次/d,连续6 d;空白组与模型组灌胃平行给予同体积生理盐水。
2.2 生化指标测定
末次给药前大鼠禁食不禁水18h,给药1h后,股动脉取血,离心后取血清,测定丙氨酸氨基转移酶(alanine aminotransferase, ALT)、天冬氨酸氨基转氨酶(aspartate aminotransferase, AST)、碱性磷酸酶(alkaline phosphatase, ALP)、透明质酸(hyaluronic acid, HA)、总胆红素(total bilirubin, TBIL)、γ-谷氨酰转移酶(γ-glutamyltransferase, GGT)、总蛋白(total protein, TP)、白蛋白(albumin, ALB)、球蛋白(globulin, GLO)、白球蛋白(A/G)比值、尿素(carbamide,UREA)、层粘蛋白(laminin, LN)、层粘蛋白(laminin, LN)、尿素氮(urea nitrogen, BUN)、肌酐(creatinine, CREA)、转化生长因子-β1(transforming growth factor β1, TGF-β1)等。
2.3 组织病理检测
实验结束后处死动物,剖腹取肝脏,用冰生理盐水清洗血迹,滤纸吸尽表面水分,精确称重,然后切取左叶肝脏固定于10%福尔马林液中常规脱水,石蜡包埋,5μm切片,采用HE常规染色,光镜下观察组织病理变化情况。
2.4 数据处理
实验数据以
3. 结果
3.1 动物一般状况变化
正常大鼠给予大黄总蒽醌提取物后出现了不同程度的排稀便,软便,被毛脏乱、红染,尿液棕黄色,低剂量组改变相对较轻;给予总鞣质提取物的大鼠粪便相对较干燥,并随给药时间延长大便逐渐呈灰暗色。各给药组大鼠活动状态无显著变化,体重随剂量增加略有变化但无显著性改变。
模型组大鼠以CCl4造模数天后,均表现出毛泽灰暗,饮食量减少,萎靡少动,抓持力弱,体重增长缓慢等现象。模型大鼠给予总蒽醌提取物后出现不同程度的排稀便、软便,被毛脏乱、红染,尿液棕黄色;给予总鞣质提取物的大鼠粪便干燥、颜色呈灰暗色,其中鞣质高剂量组动物体重恢复情况较差。
3.2 血清生化指标变化
不同实验组大鼠显著性变化的生化指标见表1,其中只是列出一部分相关生化指标。各正常动物组在给药第6天末,与空白组比较,NA2组动物血清HA,NT2组动物血清AST、ALT、HA具有明显差异(P<0.05)。与NA2组比较,NT2组动物血清AST明显升高(P<0.05)。
各模型动物组在给药6天后,与N组比较,M组动物血清AST、ALT、ALP、HA、LN、TGF-β1均显著增高(P<0.05,P<0.01);与M组比较,MA1、MA2、MT1组动物血清AST、ALT、HA、TGF-β1,MT2组动物血清AST、ALT、ALP均显著降低(P<0.05,P<0.01);与MT1组比较,MA1组动物血清HA、TGF-β1降低明显(P<0.05,P<0.01);与MT2组比较,MA2组动物血清AST、HA、TGF-β1降低明显(P<0.05,P<0.01)。
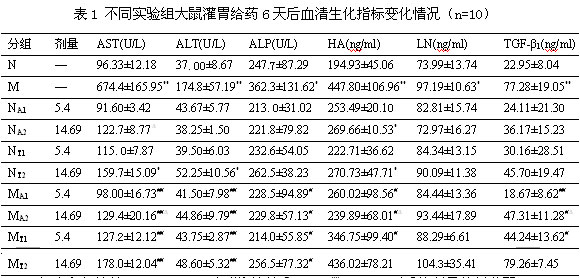
与空白组比较,*:P<0.05,**:P<0.01;与模型组比较,#:P<0.05;##:P<0.01;与同等剂量的总蒽醌给药组比较,Δ:P<0.05;ΔΔ:P<0.01
3.3 肝组织病理变化
与N组比较,NA1组肝小叶结构基本正常,部分肝细胞肿胀;NA2组肝小叶结构基本正常,肝细胞核深染,胞浆嗜酸性染色,肝细胞轻度肿胀;NT1组部分肝细胞嗜酸性变,细胞核增大,深染,可见肝细胞点状坏死;NT2组肝包膜附近可见小片状胆汁淤积,肝细胞小片状坏死,中央静脉周围肝细胞脂肪变性。
M组动物可见肝细胞弥漫性水样变性,部分肝组织大片状坏死,肝包膜处肝细胞变性、坏死,包膜下可见纤维肉芽肿及多核巨细胞,汇管区及包膜可见纤维组织增生,部分肾曲管轻度肿胀、变性。于M组比较,MA1组肝细胞见散在的空泡变性;MA2组肝细胞轻度肿胀,偶见汇管区炎症反应及小胆管增生;MT1组肝实质细胞可见散在小脂滴,部分肝细胞嗜酸性变,偶见小片状肝坏死及炎症细胞浸润,可见多核巨细胞;MT2组可见肝包膜增厚,包膜下肝细胞变性,汇管区周围肝细胞嗜酸性变性,部分肝细胞坏死,汇管区可见轻度的纤维组织增生。
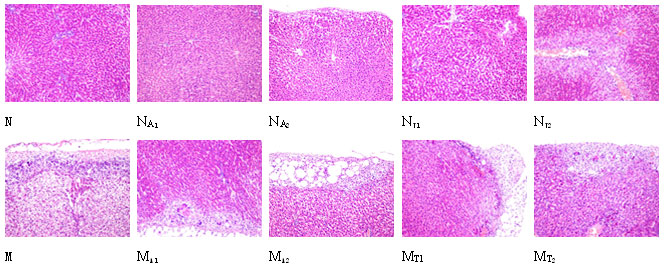
图1 正常和肝损伤模型大鼠灌胃大黄总蒽醌和总鞣质的肝脏病理切片照片HE×200
3.4 因子分析结果
针对上述给药后变化明显的6个生化指标,采用因子分析研究大黄蒽醌和鞣质对肝脏的作用规律。因子分析模型的KMO(Kaiser-Meyer-Olkin)值大于0.5,Bartlett's检验P值小于0.0001,证明所建数学模型满足可靠性检验要求。根据特征值大于1的判据[14],因子分析共提取到2个公因子,积累贡献率86.1%,表明2个公因子代表了原始数据86.1%的信息,因子载荷、特征值及积累贡献率见表2。以因子载荷大于0.5为显著性判据,公因子1主要由TGF-β1、HA、LN决定;公因子2主要由AST、ALT、ALP决定。HA和LN是肝细胞外基质代谢过程中的产物,是肝纤维化和基质沉积相关的直接指标[15],TGF-β1水平可反映慢性肝病纤维化中组织炎症坏死及纤维化程度[16-17],提示公因子1可解释为肝纤维化因子;AST、ALT和ALP反映肝细胞损伤程度[18],提示公因子2可解释为肝细胞损伤因子。根据因子分析模型,大黄总蒽醌和总鞣质对正常和肝损伤大鼠的作用规律见图2。
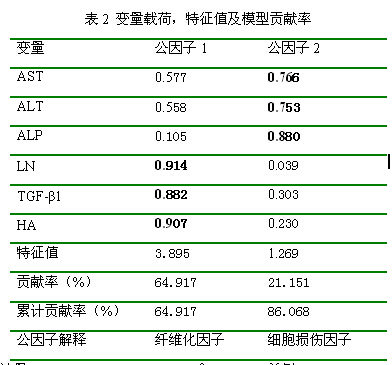
注:KMO统计量=0.567>0.5,Bartlett's Test χ2=97.479,单侧P<0.0001

图2 大黄蒽醌与鞣质部位量-效/毒关系变化的因子荷载图
4. 讨论
本文在可比剂量下,对比了大黄蒽醌和鞣质类成分对肝脏的作用规律,综合生化和病理结果表明:(1)大黄总蒽醌对肝损伤大鼠有显著的治疗效果,具体表现为显著降低血清ALT、AST、ALP,同时显著改善了肝组织坏死和炎症,与炎症和纤维化有关的血清HA和TGF-β1也显著降低。对比不同剂量组可见,蒽醌低剂量组疗效比高剂量组好,提示大黄蒽醌治疗肝病应注意选择合适的剂量。(2)与可比剂量的总蒽醌相比,大黄总鞣质对肝损伤大鼠治疗效果较差,表现为肝组织病理学改善不明显,对AST、HA、LN和TGF-β1的改善效果显著低于可比剂量的总蒽醌组。对比不同剂量组可见,鞣质高剂量组疗效比低剂量组差,肝组织病理表现甚至比模型动物对照组更差。(3)大黄总蒽醌对正常大鼠肝脏功能和组织病理学基本没有影响,而高剂量大黄总鞣质可引起正常动物ALT、AST、HA、LN和TGF-β1显著升高,肝组织病理检查可见显著损伤,提示大黄鞣质对肝脏的损伤作用大于蒽醌。
为了进一步综合且直观地展现大黄蒽醌和鞣质对正常和肝损伤大鼠的作用规律,采用因子分析方法提取了生化指标的2个公因子:公因子1(肝纤维化因子)和公因子2(肝细胞损伤因子)。从公因子变化轨迹(图2)可以直观看出大黄蒽醌和鞣质对肝脏的量-效/毒关系变化趋势:(1)与N组相比,大黄总鞣质随剂量增加,沿着纤维化方向与细胞损伤方向逐渐偏离,以纤维化方向明显,说明大黄鞣质会影响正常大鼠的肝功能。(2)与M组相比,在肝细胞损伤因子方向,大黄总鞣质不同程度地促进了细胞损伤恢复,而在肝纤维化因子方向,低剂量大黄鞣质有一定的抗纤维化作用,高剂量却进一步加重了模型动物的肝纤维化程度,提示鞣质类成分是大黄肝损伤作用的主要物质。(3)与鞣质给药组相比,正常动物给予大黄蒽醌后,无论在细胞损伤因子还是纤维化因子都表现出更低的损伤作用。模型动物给予蒽醌后,在细胞损伤因子方向明显促进了细胞损伤恢复,在肝纤维化因子方向也表现出明显的抗纤维化作用,提示蒽醌类成分是大黄保肝作用的主要物质。
文献报道大黄蒽醌类成分可以阻断实验动物组织纤维化进程[19,20]。肝纤维化是由各种致病因子所致肝内结缔组织异常增生,导致肝内纤维性细胞外基质(fibrillar extracellular matrix, ECM)过度沉积的病理过程。肝星型细胞(hepatic stellate cell, HSC)的激活与细胞外基质成分(ECM)生成过多和降解不足是肝纤维化形成的主要环节[21]。TGF-β1能激活HSC,促进激活的HSC存活,刺激HSC转化、增值和合成ECM,同时抑制ECM的降解,导致肝纤维化,ECM是已知最强的促进肝纤维化细胞因子[22,23]。正常的肝细胞无TGF-β1的表达,一旦肝脏受损,血小板、巨噬细胞、库普弗细胞等激活后释放出TGF-β1。大黄素和大黄酸等蒽醌类物质能够抑制TGF-β1的表达,从而抑制HSC的活化,阻止肝纤维化的发生[24,25],推测是大黄保肝作用的重要机制。
鞣质又称单宁,是一类比较复杂的多元酚类化合物,分为可水解鞣质和缩合鞣质两大类[26]。鞣质的肝毒性多有报道,但研究较为薄弱,一般认为可水解鞣质的肝毒性较大。大黄鞣质主要为可水解鞣质类。本实验结果显示,高剂量大黄鞣质可引起肝损伤,且主要是沿着纤维化方向发展。大黄鞣质肝毒性研究较少,应引起关注深入研究并阐明其诱发肝纤维化损伤的分子机制。大黄鞣质主要是由没食子酸和儿茶素为基本单元结合或缩合形成的系列衍生物,一般认为没食子酸的肝毒性大于儿茶素,大黄鞣质的主要毒性成分及构-毒关系需要深入研究。
蒽醌和鞣质是大黄中最重要的两类活性成分。本文结果提示在一定的剂量范围,大黄蒽醌和鞣质对肝脏表现出相反的作用,蒽醌保肝、鞣质伤肝;而笔者课题组前期研究还发现,大黄蒽醌和鞣质对胃肠道也具有相反的作用,蒽醌致泻、鞣质止泻 [27],说明大黄具有双向作用的特点。由于组成成分复杂,很多中药都存在双向作用[28],如人参既能升压又能降压[29],人参所含不同皂苷类成分表现出促进血管生成和抑制血管生成的相反作用[30],三七能止血又能活血[31]等。有学者将中药的双向作用称为阴阳作用[9,30]。本文采用因子分析方法,直观反映出了大黄蒽醌与鞣质对肝脏的阴/阳矛盾作用,为研究大黄的效/毒双向作用提供了有益参考。
笔者前期研究大黄总提物对肝脏的双向作用发现[13],大黄在一定剂量下对正常动物表现出肝损伤作用,但对于肝损伤模型动物则表现出治疗作用,符合《黄帝内经》“有故无殒”思想对药物毒性作用的认识,即是指当药物选择对证(病),不仅不会发生毒性作用,还可以有效治疗疾病[32],但该研究未设计实验探讨大黄“有故无殒”现象的物质基础。本实验在“有故无殒”思想指导下,采用肝损伤模型动物与正常动物对比考察大黄致肝损伤的化学成分,发现大黄总鞣质提取物是引起大鼠肝损伤的主要成分,总蒽醌提取物是肝保护作用的主要成分。与前期大黄总提物的实验比较[13],将大黄鞣质和蒽醌分开后,大黄鞣质引起大鼠肝损伤所需的用药周期比大黄总提物更短、且损伤更明显,推测原因可能是总提物中蒽醌成分的肝保护作用拮抗了鞣质成分的肝损伤作用。因此大黄在临床治疗肝病时,应注意设法减少对鞣质成分的煎出和提取,避免鞣质类成分对疗效的影响和潜在的肝毒性。中药不同组分间拮抗作用对临床疗效和安全性可能产生的影响尚未得到充分重视,应加强研究,提高中药临床合理用药水平。
参考文献
[1] 国家药典委员会. 中华人民共和国药典2010 年版[M]. 一部. 北京:中国医药科技出版社,2010: 22.
[2] W.Y.Wen, J.Ouyang, X.H.Xiao,et al. Antimicrobial properties and toxicity of anthraquinones by microcalorimetric bioassay[J]. Chinese Journal of Chemistry, 2006,24(1):45-50.
[3]任红兵,王艳艳,王团结.大黄总蒽醌对大鼠急性肾毒性研究[J]. 辽宁中医药大学学报, 2012,14(1):69-71.
[4]笪红远,江振洲,王翠芬,等.大黄酸和大黄素在体外对人肾小管上皮细胞的毒性作用研究[J].中草药, 2009,40(1):102 -105.
[5]傅兴圣,陈菲,刘训红,等.大黄化学成分与药理作用研究新进展[J]. 中国新药杂志, 2011 ,20(16):1534-1538.
[6]王伽伯, 马永刚, 张 萍,等.炮制对大黄化学成分和肝肾毒性的影响及其典型相关分析[J].药学学报, 2009,44( 8) : 885- 890.
[7] 邢晶晶,曹婷婷,杨帆,等.鞣质类化合物研究的进展情况[J].黑龙江医药, 2011,24( 5) : 776 -780.
[8]杜国成.中药鞣质成分的药理作用探析[J].中国医药科学, 2000,17( 1) : 27-33.
[9]Ling-na Zeng,Zhi-jie Ma,Jia-bo Wang,et al. The protective and toxic effects of rhubarb tannins and anthraquinones in treating hexavalent chromium-injured rats: The Yin/Yang actions of rhubarb[J]. Journal of Hazardous Materials, 2013,246-247:1-9.
[10]孙玉琦, 肖小河, 马永刚,等. 大黄煎煮过程中蒽醌类成分动态变化规律研究[J]. 解放军药学学报,2006,22(4): 281.
[11] 国家药典委员会.中华人民共和国药典2005 年版[M].一部.北京:中国医药科技出版社,附录XB“鞣质含量测定法”.
[12]J.B. Wang, Y. Qin, W.J. Kong, et al. Identification of the antidiarrhoeal components in official rhubarb using liquid chromatography–tandem mass spectrometry[J]. Food Chemistry, 2011,129(4):1737–1743.
[13]J.B. Wang, H.P. Zhao, Y.L. Zhao, et al. Hepatotoxicity or hepatoprotection? Pattern recognition for the paradoxical effect of the Chinese herb Rheum palmatum L. in treating rat liver injury[J]. PLoS ONE, 2011, 6(9):e24498 doi:10.1371/journal.pone.0024498.
[14] Sharma S. Applied Multivariate Techniques[M]. New York: Wiley 1996,90-143.
[15] Miele L, Forgione A, La Torre G, et al. Serum levels of hyaluronic acid and tissue metalloproteinase inhibitor-1 combined with age predict the presence of nonalcoholic steatohepatitis in a pilot cohort of subjects with nonalcoholic fatty liver disease[J]. Transl Res ,2009, 154(4): 194-201.
[16] 党双锁, 李亚萍. TGF-β1在纤维化研究中的新进展[J]. 中国病理生理杂志,2007,23(12): 2405- 2409.
[17] 邵祥强,肖华胜. 肝纤维化发病机制与临床诊断的研究进展[J].世界华人消化杂志, 2011,19(3):268-274.
[18]张洁,曹芸,王之青,等. 常规生化指标评估慢性肝功能损害的临床应用价值[J].胃肠病学,2008,13(10) : 620 -622.
[19]Dong MX, Jia Y, Zhang YB,et al. Emodin protects rat liver from CCl4-induced fibrogenesis via inhibition of hepatic stellate cells activation[J]. World Journal of Gastroenterology , 2009, 15(38): 4753-4762 .
[20]田 瑗,郭晓琳,王丽强,等.大黄素对TNBS诱导大鼠肠纤维化的影响[J].世界华人消化杂志, 2012,20(28): 2703-2708.
[21] Li JT ,et al. Molecular mechanism of hepatic stellate cell activation and antifibrotic therapeutic strategies[J]. J Gastroenterol, 2008, 43(6): 419-428.
[22]黄艳,黄成,李俊. 肝纤维化病程中Kupffer细胞分泌的细胞因子对肝星状细胞活化增值、凋亡的调控[J]. 中国药理学通报, 2010,26(1):9-13 .
[23] Matsuoka M ,et al. Stimulation of hepatic lipocyte collagen production by Kupffer cell-derived transforming growth factor b: implication for a pathogenetic role in alcoholic liver fibrogenesis[J]. Hepatology, 1990,11(4): 599-605.
[24] 曾嵘,王俭勤,段书众,等.大黄酸对人肾小管上皮细胞血小板反应蛋白和TGF-β1表达的影响[J].肾脏病与透析肾移植杂志, 2008,17( 3) : 249-251.
[25]J-M Zheng, J-M Zhu, L-S Li and Z-H Liu. Rhein reverses the diabetic phenotype of mesangial cells over-expressing the glucose transporter (GLUT1) by inhibiting the hexosamine pathway[J]. British Journal of Pharmacology, 2008,153(7):1456–1464.
[26]黄浩,巢启荣.大黄鞣质及相关物的研究概况[J].中草药,1997,29(3):199-202.
[27]Y. Qin, J.B. Wang, W.J. Kong, et al.The diarrhoeogenic and antidiarrhoeal bidirectional effects of rhubarb and its potential mechanism[J]. J Ethnopharmacol,2011,133(3): 1096-1102.
[28]张晓双,白黎明.论中药的双向调节作用[J].甘肃中医学院学报,2006,23(4):14-15.
[29] P.Y. Yue, N.K. Mak, Y.K. Cheng, et al.Pharmacogenomics and the Yin/Yang actions of ginseng: anti-tumor, angiomodulating and steroid-like activities of ginsenosides[J]. Chinese Medicine, 2007,2:6 doi:10.1186/1749-8546-2-6.
[30]S. Sengupta, S.A. Toh, L.A. Sellers,et al. Modulating angiogenesis: the yin and the yang in ginseng[J]. Circulation,2004, 110 (10):1219-1225.
[31] T. B. Ng. Pharmacological activity of sanchi ginseng (Panax notoginseng) [J].Journal of Pharmacy and Pharmacology,2006,58:1007-1019.
[32] M. Ni, The Yellow Emperor’s Classic of Medicine: A new translation of the Neijing Suwen with commentary[M], Shambhala, Boston, 1995.
北京药学会 地址:北京市朝阳区北三环中路2号小二楼2层
本网站浏览66554378次
Copyright 2012 北京药学会( 本网站所有内容未经许可,不得以任何形式进行转载 ) All Rights Reservered